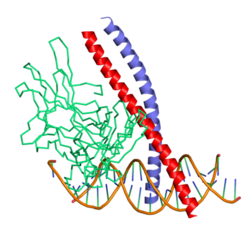
c-Jun
c-Junは、ヒトではJUN遺伝子にコードされるタンパク質である。c-Junはc-Fosとともに、初期応答転写因子AP-1を形成する。c-JunはFos結合タンパク質p39として同定され、後にJUN遺伝子の産物として再発見された。c-Junは最初に発見された発がん性転写因子である[5]。c-Junはウイルス性がんタンパク質v-Junの細胞ホモログである[6]。ウイルスホモログであるv-Junはトリ肉腫ウイルスavian sarcoma virus 17に発見され、Junという名称は日本語の「じゅうなな」(17)に由来する[7]。ヒトのJUN遺伝子にコードされるタンパク質はこのウイルスタンパク質と高度に類似しており、遺伝子発現を調節する特定のDNA配列と直接相互作用する。JUN遺伝子はイントロンを持たない遺伝子であり、ヒトの悪性腫瘍における転座や欠失の双方と関係している染色体領域1p32-p31にマッピングされている[8]。
機能
編集調節
編集AP-1を形成するc-Junとその二量体化パートナーの双方が、成長因子、炎症性サイトカイン、酸化ストレスやその他の細胞ストレス、紫外線照射など多様な細胞外刺激による調節を受けている。一例として、紫外線照射はc-Junの発現の強力な誘導因子となる[6]。
他の最初期遺伝子と同様、JUNの転写誘導は細胞内の既存のタンパク質を用いて行われ、タンパク質合成が実験的に遮断されている場合でも誘導は行われる[9]。
JUNの転写は自身の産物による自己調節を受けている。JUNのプロモーター領域内の高親和性AP-1結合部位にc-Jun(AP-1)が結合することで、JUNの転写は誘導される。こうした正の自己調節は、細胞外刺激由来のシグナルを延長するための機構の1つとなっている可能性がある。この機構は、がんにおけるc-Jun活性の生物学的重要性をもたらしている場合がある[10][11]。
また、c-Junの活性はERK経路によっても調節される。ERKの恒常的活性化はJUNの転写を高め、またCREBやGSK3を介してc-Junの安定性を高めることが知られている。その結果、c-Jun、そしてRACK1、サイクリンD1といった下流標的の活性化が引き起こされる。RACK1はJNKの活性を高め、JNKシグナルを活性化することでc-Junの活性を調節する[12]。.
c-Junのセリン63番、73番、そしてスレオニン91番、93番のリン酸化によって、c-Jun標的遺伝子の転写は高まる[13]。このc-Jun活性の調節はJNKによって行われる。ストレス誘発性のアポトーシスや細胞増殖の際のc-Junの活性は、このN末端のリン酸化によって調節されていることが示されている[14]。他の研究では、RasやFosによる発がん性形質転換の際にもセリン63番、73番のリン酸化が必要となることが示されている[15]。
細胞周期の進行
編集c-Junは細胞周期のG1期の通過に必要であることが研究から示されており、c-Junヌル変異細胞の細胞周期はG1期で停止する。c-JunはRbのリン酸化(不活性化)をもたらす主要な因子であるサイクリンD1の転写レベルを調節している。c-JunはサイクリンD1を介したキナーゼ活性を十分なレベルに維持し、細胞周期の進行を可能にしている[6]。
c-Junが存在しない細胞ではp53(細胞周期の停止の誘導因子)とp21(CDK阻害因子でありp53の標的遺伝子)の発現が上昇し、細胞周期の進行に欠陥が生じる。一方c-Junの過剰発現はp53やp21の減少をもたらし、細胞増殖が加速する。c-Junはp53遺伝子のプロモーター内のvariant AP-1 siteに結合することでp53の転写を抑制し、p53をダウンレギュレーションすることで細胞周期の進行を制御している[16]。
抗アポトーシス活性
編集紫外線照射は、c-Junの発現とJNKシグナル伝達経路を活性化する。c-Junは紫外線誘発性アポトーシスから細胞を保護し、NF-κBと競合することでTNFαによって誘導されるアポトーシスを防いでいる。c-Junによるアポトーシスからの保護にはセリン63/73番(c-Junのリン酸化に関与している)が必要であるが、これらの残基はG1期の進行には必要ではない。このことは、c-Junによる細胞周期の進行とアポトーシスの防止は2つの異なる機構によって調節されていることを示唆している[6]。
肝細胞癌における研究では、c-Junの不活性化によってp53タンパク質やp53標的遺伝子であるNOXAのmRNA濃度の上昇と相関した形で腫瘍発生が損なわれることが示されている。また、c-Junは肝細胞をアポトーシスから防ぐ役割を果たしており、c-Junを欠く細胞はTNFαによるアポトーシスに対する感受性が高まる。こうしたc-Junを欠く肝細胞では、p53の欠失によってTNFαに対する抵抗性を回復する。これらの結果は、肝腫瘍においてc-Junがp53のアポトーシス促進活性に対抗する役割を果たしていることを示している[17]。
臨床的意義
編集c-Junは月経周期を通じて子宮内膜の細胞増殖とアポトーシスに関与していることが知られている。c-Junのタンパク質濃度の周期的変化は、腺上皮細胞の増殖とアポトーシスに重要である。間質細胞でのc-Junの持続的発現は、分泌期後期におけるアポトーシスの開始を妨げる可能性がある[18]。
がん
編集非小細胞肺癌(NSCLC)を用いた研究では、原発性・転移性肺腫瘍症例の31%でc-Junの過剰発現が観察されるのに対し、正常な気道や肺胞の上皮細胞は一般的にはc-Junを発現していない[19]。
浸潤性乳がん103症例についての研究では、活性化されたc-Junは主に乳がんの浸潤先進部に発現しており、増殖や血管新生と関連していることが示されている[20]。
発がんイニシエーション
編集肝細胞癌を化学的に誘発したマウスにおいて腫瘍発生のさまざまな段階でc-Junを肝特異的に不活性化した研究では、c-Junは腫瘍発生の初期段階に必要であり、c-Junの欠失によって腫瘍形成が大きく抑制されることが示されている。また、c-Junはイニシエーションとプログレッション過程間での腫瘍細胞の生存にも必要である。対照的に、進行した腫瘍ではc-Junの不活性化によって腫瘍のプログレッションが損なわれることはない[17]。
乳がん
編集MCF-7細胞におけるc-Junの過剰発現は全体的なaggressivenessの増大をもたらし、細胞運動性の増大、細胞外マトリックス分解酵素MMP-9の発現上昇、in vitroでのchemoinvasionの増大、ヌードマウスにおける外因性エストロゲンの非存在下での腫瘍形成が観察される。c-Junを過剰発現したMCF-7細胞はエストロゲンやタモキシフェンへの応答性を失うため、c-Junの過剰発現は乳がん細胞にエストロゲン非依存性表現型をもたらすと考えられている。c-Junを過剰発現したMCF-7細胞で観察される表現型は、進行してホルモン不応性となった乳がんで臨床的に観察されるものと類似している[21]。
c-Junの過剰発現による浸潤性表現型は他の研究でも確認されている。この研究では、c-Junを過剰発現した乳がんではin vivoでの肝転移の増大も示されており、c-Junが乳がんの転移に重要な役割を果たしていることが示唆されている[22]。
乳がんでは、ErbB2誘発性の乳腺上皮細胞の遊走と浸潤において、内因性のc-Junが重要な役割を果たしていることが知られている。c-JunはSCFやCCL5のプロモーターを活性化し、発現誘導されたSCFやCCL5は乳腺上皮細胞集団の自己複製を促進する。このことは、c-Junが乳がん幹細胞の増殖を媒介し、腫瘍の浸潤性を高めていることを示唆している[23]。
外陰がん
編集外陰部扁平上皮癌試料では、RARBがん抑制遺伝子の高メチル化による不活性化と関連して、c-Junの過剰発現が観察される[10]。外陰がん試料では正常な皮膚や前がん病変と比較してc-JunのmRNA濃度が高く、発がんにおけるRARBとc-Junの関連が強く示唆される[10]。
細胞分化
編集10種類の未分化型でaggressivenessの高い肉腫では、JUN遺伝子の増幅やc-JunのmRNA・タンパク質双方の過剰発現が示されている。ヒト脂肪肉腫と類似した非腫瘍性の脂肪前駆細胞株である3T3-L1細胞では、c-Junの過剰発現によって脂肪細胞への分化が遮断されるもしくは遅れる[24]。
神経や脊髄の再生
編集齧歯類では、末梢神経の損傷によってJNKシグナルが迅速によって活性化され、その結果c-Junが活性化される。一方、中枢神経系の損傷ではこうした応答は起こらない。c-Junは末梢神経系と中枢神経系の双方において軸索の再生促進の十分因子であり、後根神経節ニューロンと皮質ニューロンの双方でc-Junの過剰発現によって再生の増大が引き起こされることが示されている[25]。
抗がん剤標的として
編集c-Junはがんにおいて過剰発現が観察されるため[10]、いくつかの研究ではc-Junのがん治療標的としての可能性が提唱されている。ある研究では、RasやFosが発がん性形質転換を引き起こすためにはJNKによるc-Junのセリン63番、73番のリン酸化が必要であることが示されている。この研究では、これらN末端のリン酸化が行われないc-Jun変異体マウスでは皮膚腫瘍や骨肉腫を誘発した際の腫瘍発生が損なわれることが示されている[15]。また、大腸がんモデルマウスではc-JunのN末端のリン酸化不能変異または腸特異的なc-Junの不活性化によってがんの発生が低下し、寿命が伸長する[13]。そのため、c-JunのN末端のリン酸化(もしくはJNKシグナル伝達経路)の標的化は、腫瘍の成長を阻害する戦略の1つとなる可能性がある。
メラノーマ由来B16-F10がん細胞では、JunBのノックダウンとJNK/c-Junの薬理的不活性化を組み合わせることで細胞毒性が引き起こされ、細胞周期の停止とアポトーシスにつながる。このJunBとc-Junを標的とした戦略によって腫瘍細胞接種マウスの生存が改善することから、抗がん戦略としての可能性が示唆される[26]。
抗がん作用
編集大部分の研究結果は、c-Junが腫瘍のイニシエーションや浸潤性の増大に寄与することを示していている。しかしながら、いくつかの研究ではc-Junの代替的な活性が発見されており、c-Junは実際にはがんにとって諸刃の剣となっている可能性が示唆されている[27]。
p16
編集p16INK4aは細胞周期の進行を阻害するがん抑制因子である。ある研究では、c-Junがp16INK4aの遺伝子のプロモーターのメチル化を阻害し、p16INK4aの遺伝的サイレンシングを防いでいることが示されている[28]。
チロホリン
編集チロホリン(tylophorine)は、細胞周期の停止を誘導することで抗がん作用を示す植物由来アルカロイドの一種である。チロホリン処理はc-Junタンパク質の蓄積を高めることが研究で示されている。c-Junの発現はチロホリンとともにサイクリンA2をダウンレギュレーションすることで、がん細胞の細胞周期のG1期での停止を促進する。これらの結果はチロホリンの抗がん作用がc-Junによって媒介されていることを示唆している[29]。
相互作用
編集c-Junは次に挙げる因子と相互作用する。
- ATF2[30][31][32]
- AR[33]
- ASCC3[34]
- ATF3[32][35][36]
- BCL3[37]
- BCL6[38]
- BRCA1[39]
- c-Fos[40][41][42][43][44][45][46]
- CSNK2A1[47]
- COPS5[48]
- CREBBP[49]
- CSNK2A2[47]
- DDX21[50]
- DDIT3[51]
- ERG[52]
- ETS2[53]
- FOSL1[41]
- GTF2B[54]
- MAPK8[55][56][57][58][59][60][61][62]
- MyoD[63]
- NACA[64]
- NELFB[65]
- NFE2L1[46]
- NFE2L2[46]
- NCOR2[66]
- NCOA1[67][68][69]
- PIN1[70]
- RBM39[71]
- RELA[43]
- RB1[72]
- RFWD2[73][74]
- RUNX1[75][76]
- RUNX2[75][76]
- SMAD3[77][78][79]
- STAT1[80]
- STAT3[80]
- TBP[54]
- TGIF1[81]
出典
編集- ^ a b c GRCh38: Ensembl release 89: ENSG00000177606 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000052684 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ “Fortuitous convergences: the beginnings of JUN”. Nature Reviews. Cancer 2 (6): 465–9. (June 2002). doi:10.1038/nrc818. PMID 12189388.
- ^ a b c d “c-Jun regulates cell cycle progression and apoptosis by distinct mechanisms”. The EMBO Journal 18 (1): 188–97. (January 1999). doi:10.1093/emboj/18.1.188. PMC 1171114. PMID 9878062.
- ^ “Avian sarcoma virus 17 carries the jun oncogene”. Proceedings of the National Academy of Sciences of the United States of America 84 (9): 2848–52. (May 1987). Bibcode: 1987PNAS...84.2848M. doi:10.1073/pnas.84.9.2848. PMC 304757. PMID 3033666.
- ^ “Entrez Gene: JUN jun oncogene”. 2024年8月16日閲覧。
- ^ “Gene regulation in the immediate-early response process”. Advances in Biological Regulation 62: 37-49. (2016). doi:10.1016/j.jbior.2016.05.001. PMID 27220739.
- ^ a b c d “Association of Retinoic Acid Receptor β Gene With Onset and Progression of Lichen Sclerosus-Associated Vulvar Squamous Cell Carcinoma”. JAMA Dermatology 154 (7): 819–823. (July 2018). doi:10.1001/jamadermatol.2018.1373. PMC 6128494. PMID 29898214.
- ^ “The jun proto-oncogene is positively autoregulated by its product, Jun/AP-1”. Cell 55 (5): 875–85. (December 1988). doi:10.1016/0092-8674(88)90143-2. PMID 3142689.
- ^ “Rewired ERK-JNK signaling pathways in melanoma”. Cancer Cell 11 (5): 447–60. (May 2007). doi:10.1016/j.ccr.2007.03.009. PMC 1978100. PMID 17482134.
- ^ a b “Interaction of phosphorylated c-Jun with TCF4 regulates intestinal cancer development”. Nature 437 (7056): 281–5. (September 2005). Bibcode: 2005Natur.437..281N. doi:10.1038/nature03914. PMID 16007074.
- ^ “Amino-terminal phosphorylation of c-Jun regulates stress-induced apoptosis and cellular proliferation”. Nature Genetics 21 (3): 326–9. (March 1999). doi:10.1038/6854. PMID 10080190.
- ^ a b “Oncogenic transformation by ras and fos is mediated by c-Jun N-terminal phosphorylation”. Oncogene 19 (22): 2657–63. (May 2000). doi:10.1038/sj.onc.1203603. PMID 10851065.
- ^ “Control of cell cycle progression by c-Jun is p53 dependent”. Genes & Development 13 (5): 607–19. (March 1999). doi:10.1101/gad.13.5.607. PMC 316508. PMID 10072388.
- ^ a b “Liver tumor development. c-Jun antagonizes the proapoptotic activity of p53”. Cell 112 (2): 181–92. (January 2003). doi:10.1016/S0092-8674(03)00042-4. PMID 12553907.
- ^ “The role of c-jun protein in proliferation and apoptosis of the endometrium throughout the menstrual cycle”. Gynecologic and Obstetric Investigation 57 (3): 121–6. (2004). doi:10.1159/000075701. PMID 14691341.
- ^ “Altered cJUN expression: an early event in human lung carcinogenesis”. Cancer Research 56 (2): 305–15. (January 1996). PMID 8542585.
- ^ “c-Jun activation is associated with proliferation and angiogenesis in invasive breast cancer”. Human Pathology 37 (6): 668–74. (June 2006). doi:10.1016/j.humpath.2006.01.022. PMID 16733206.
- ^ “cJun overexpression in MCF-7 breast cancer cells produces a tumorigenic, invasive and hormone resistant phenotype”. Oncogene 18 (44): 6063–70. (October 1999). doi:10.1038/sj.onc.1202989. PMID 10557095.
- ^ “Critical role of c-Jun overexpression in liver metastasis of human breast cancer xenograft model”. BMC Cancer 7: 145. (August 2007). doi:10.1186/1471-2407-7-145. PMC 1959235. PMID 17672916.
- ^ “c-Jun induces mammary epithelial cellular invasion and breast cancer stem cell expansion”. The Journal of Biological Chemistry 285 (11): 8218–26. (March 2010). doi:10.1074/jbc.M110.100792. PMC 2832973. PMID 20053993.
- ^ “JUN oncogene amplification and overexpression block adipocytic differentiation in highly aggressive sarcomas”. Cancer Cell 11 (4): 361–74. (April 2007). doi:10.1016/j.ccr.2007.02.007. PMID 17418412.
- ^ “Intrinsic mechanisms of neuronal axon regeneration” (英語). Nature Reviews. Neuroscience 19 (6): 323–337. (June 2018). doi:10.1038/s41583-018-0001-8. PMC 5987780. PMID 29666508.
- ^ “Targeting c-Jun and JunB proteins as potential anticancer cell therapy”. Oncogene 27 (5): 641–52. (January 2008). doi:10.1038/sj.onc.1210690. PMID 17667939.
- ^ “AP-1: a double-edged sword in tumorigenesis”. Nature Reviews. Cancer 3 (11): 859–868. (November 2003). doi:10.1038/nrc1209. PMID 14668816.
- ^ Kollmann, Karoline; Heller, Gerwin; Sexl, Veronika (2011-05). “c-JUN prevents methylation of p16(INK4a) (and Cdk6): the villain turned bodyguard”. Oncotarget 2 (5): 422–427. doi:10.18632/oncotarget.279. ISSN 1949-2553. PMC 3248190. PMID 21789792.
- ^ “c-Jun-mediated anticancer mechanisms of tylophorine”. Carcinogenesis 34 (6): 1304–14. (June 2013). doi:10.1093/carcin/bgt039. PMID 23385061.
- ^ “Interaction of nuclear proteins with an AP-1/CRE-like promoter sequence in the human TNF-alpha gene”. Journal of Leukocyte Biology 56 (1): 27–35. (July 1994). doi:10.1002/jlb.56.1.27. PMID 8027667.
- ^ “A cDNA for a human cyclic AMP response element-binding protein which is distinct from CREB and expressed preferentially in brain”. Molecular and Cellular Biology 10 (4): 1347–57. (April 1990). doi:10.1128/MCB.10.4.1347. PMC 362236. PMID 2320002.
- ^ a b “Cross-family dimerization of transcription factors Fos/Jun and ATF/CREB alters DNA binding specificity”. Proceedings of the National Academy of Sciences of the United States of America 88 (9): 3720–4. (May 1991). Bibcode: 1991PNAS...88.3720H. doi:10.1073/pnas.88.9.3720. PMC 51524. PMID 1827203.
- ^ “Androgenic induction of prostate-specific antigen gene is repressed by protein-protein interaction between the androgen receptor and AP-1/c-Jun in the human prostate cancer cell line LNCaP”. The Journal of Biological Chemistry 272 (28): 17485–94. (July 1997). doi:10.1074/jbc.272.28.17485. PMID 9211894.
- ^ “Novel transcription coactivator complex containing activating signal cointegrator 1”. Molecular and Cellular Biology 22 (14): 5203–11. (July 2002). doi:10.1128/MCB.22.14.5203-5211.2002. PMC 139772. PMID 12077347.
- ^ “ATF3 enhances c-Jun-mediated neurite sprouting”. Brain Research. Molecular Brain Research 120 (1): 38–45. (December 2003). doi:10.1016/j.molbrainres.2003.09.014. PMID 14667575.
- ^ “Analysis of ATF3, a transcription factor induced by physiological stresses and modulated by gadd153/Chop10”. Molecular and Cellular Biology 16 (3): 1157–68. (March 1996). doi:10.1128/MCB.16.3.1157. PMC 231098. PMID 8622660.
- ^ “Bcl3, an IkappaB protein, stimulates activating protein-1 transactivation and cellular proliferation”. The Journal of Biological Chemistry 274 (40): 28491–6. (October 1999). doi:10.1074/jbc.274.40.28491. PMID 10497212.
- ^ “Repression of AP-1 function: a mechanism for the regulation of Blimp-1 expression and B lymphocyte differentiation by the B cell lymphoma-6 protooncogene”. Journal of Immunology 169 (4): 1922–9. (August 2002). doi:10.4049/jimmunol.169.4.1922. PMID 12165517.
- ^ “JunB potentiates function of BRCA1 activation domain 1 (AD1) through a coiled-coil-mediated interaction”. Genes & Development 16 (12): 1509–17. (June 2002). doi:10.1101/gad.995502. PMC 186344. PMID 12080089.
- ^ “Identification of SWI.SNF complex subunit BAF60a as a determinant of the transactivation potential of Fos/Jun dimers”. The Journal of Biological Chemistry 276 (4): 2852–7. (January 2001). doi:10.1074/jbc.M009633200. PMID 11053448.
- ^ a b “Cross-family interaction between the bHLHZip USF and bZip Fra1 proteins results in down-regulation of AP1 activity”. Oncogene 14 (17): 2091–8. (May 1997). doi:10.1038/sj.onc.1201046. PMID 9160889.
- ^ “Crystal structure of the heterodimeric bZIP transcription factor c-Fos-c-Jun bound to DNA”. Nature 373 (6511): 257–61. (January 1995). Bibcode: 1995Natur.373..257G. doi:10.1038/373257a0. PMID 7816143.
- ^ a b “ERK MAP kinase links cytokine signals to activation of latent HIV-1 infection by stimulating a cooperative interaction of AP-1 and NF-kappaB”. The Journal of Biological Chemistry 274 (39): 27981–8. (September 1999). doi:10.1074/jbc.274.39.27981. PMID 10488148.
- ^ “Isolation and characterization of a novel member of the gene family encoding the cAMP response element-binding protein CRE-BP1”. The Journal of Biological Chemistry 268 (6): 4259–66. (February 1993). doi:10.1016/S0021-9258(18)53604-8. PMID 8440710.
- ^ “Detection and modulation in vivo of helix-loop-helix protein-protein interactions”. The Journal of Biological Chemistry 268 (1): 5–8. (January 1993). doi:10.1016/S0021-9258(18)54105-3. PMID 8380166.
- ^ a b c “Nrf2 and Nrf1 in association with Jun proteins regulate antioxidant response element-mediated expression and coordinated induction of genes encoding detoxifying enzymes”. Oncogene 17 (24): 3145–56. (December 1998). doi:10.1038/sj.onc.1202237. PMID 9872330.
- ^ a b “Casein kinase II interacts with the bZIP domains of several transcription factors”. Nucleic Acids Research 26 (16): 3854–61. (August 1998). doi:10.1093/nar/26.16.3854. PMC 147779. PMID 9685505.
- ^ “A new group of conserved coactivators that increase the specificity of AP-1 transcription factors”. Nature 383 (6599): 453–7. (October 1996). Bibcode: 1996Natur.383..453C. doi:10.1038/383453a0. PMID 8837781.
- ^ “CBP alleviates the intramolecular inhibition of ATF-2 function”. The Journal of Biological Chemistry 273 (44): 29098–105. (October 1998). doi:10.1074/jbc.273.44.29098. PMID 9786917.
- ^ “The DEXD/H-box RNA helicase RHII/Gu is a co-factor for c-Jun-activated transcription”. The EMBO Journal 21 (3): 451–60. (February 2002). doi:10.1093/emboj/21.3.451. PMC 125820. PMID 11823437.
- ^ “CHOP enhancement of gene transcription by interactions with Jun/Fos AP-1 complex proteins”. Molecular and Cellular Biology 19 (11): 7589–99. (November 1999). doi:10.1128/MCB.19.11.7589. PMC 84780. PMID 10523647.
- ^ “Identification of amino acid residues in the ETS transcription factor Erg that mediate Erg-Jun/Fos-DNA ternary complex formation”. The Journal of Biological Chemistry 276 (20): 17181–9. (May 2001). doi:10.1074/jbc.M010208200. PMID 11278640.
- ^ “The Ets transcription factors interact with each other and with the c-Fos/c-Jun complex via distinct protein domains in a DNA-dependent and -independent manner”. The Journal of Biological Chemistry 272 (42): 26188–95. (October 1997). doi:10.1074/jbc.272.42.26188. PMID 9334186.
- ^ a b “In vitro association between the Jun protein family and the general transcription factors, TBP and TFIIB”. The Biochemical Journal 305 (Pt 3): 967–74. (February 1995). doi:10.1042/bj3050967. PMC 1136352. PMID 7848298.
- ^ “Role of the TAB2-related protein TAB3 in IL-1 and TNF signaling”. The EMBO Journal 22 (23): 6277–88. (December 2003). doi:10.1093/emboj/cdg605. PMC 291846. PMID 14633987.
- ^ “ASK1 is essential for JNK/SAPK activation by TRAF2”. Molecular Cell 2 (3): 389–95. (September 1998). doi:10.1016/S1097-2765(00)80283-X. PMID 9774977.
- ^ “JNK1: a protein kinase stimulated by UV light and Ha-Ras that binds and phosphorylates the c-Jun activation domain”. Cell 76 (6): 1025–37. (March 1994). doi:10.1016/0092-8674(94)90380-8. PMID 8137421.
- ^ “Regulation of two JunD isoforms by Jun N-terminal kinases”. The Journal of Biological Chemistry 277 (33): 29710–8. (August 2002). doi:10.1074/jbc.M204552200. PMID 12052834.
- ^ “Critical roles of TRAF2 and TRAF5 in tumor necrosis factor-induced NF-kappa B activation and protection from cell death”. The Journal of Biological Chemistry 276 (39): 36530–4. (September 2001). doi:10.1074/jbc.M104837200. PMID 11479302.
- ^ “Interaction between c-Rel and the mitogen-activated protein kinase kinase kinase 1 signaling cascade in mediating kappaB enhancer activation”. The Journal of Biological Chemistry 271 (15): 8971–6. (April 1996). doi:10.1074/jbc.271.15.8971. PMID 8621542.
- ^ “Neither ERK nor JNK/SAPK MAP kinase subtypes are essential for histone H3/HMG-14 phosphorylation or c-fos and c-jun induction”. Journal of Cell Science 108 (Pt 11): 3599–609. (November 1995). doi:10.1242/jcs.108.11.3599. PMID 8586671.
- ^ “Mitogen-activated protein kinase kinase 7 is an activator of the c-Jun NH2-terminal kinase”. Proceedings of the National Academy of Sciences of the United States of America 94 (14): 7337–42. (July 1997). Bibcode: 1997PNAS...94.7337T. doi:10.1073/pnas.94.14.7337. PMC 23822. PMID 9207092.
- ^ “Functional antagonism between c-Jun and MyoD proteins: a direct physical association”. Cell 68 (3): 507–19. (February 1992). doi:10.1016/0092-8674(92)90187-H. PMID 1310896.
- ^ “Bone-specific expression of the alpha chain of the nascent polypeptide-associated complex, a coactivator potentiating c-Jun-mediated transcription”. Molecular and Cellular Biology 18 (3): 1312–21. (March 1998). doi:10.1128/MCB.18.3.1312. PMC 108844. PMID 9488446.
- ^ “COBRA1 inhibits AP-1 transcriptional activity in transfected cells”. Biochemical and Biophysical Research Communications 325 (2): 568–73. (December 2004). doi:10.1016/j.bbrc.2004.10.079. PMID 15530430.
- ^ “Silencing mediator of retinoic acid and thyroid hormone receptors, as a novel transcriptional corepressor molecule of activating protein-1, nuclear factor-kappaB, and serum response factor”. The Journal of Biological Chemistry 275 (17): 12470–4. (April 2000). doi:10.1074/jbc.275.17.12470. PMID 10777532.
- ^ “A nuclear factor, ASC-2, as a cancer-amplified transcriptional coactivator essential for ligand-dependent transactivation by nuclear receptors in vivo”. The Journal of Biological Chemistry 274 (48): 34283–93. (November 1999). doi:10.1074/jbc.274.48.34283. PMID 10567404.
- ^ “Activating protein-1, nuclear factor-kappaB, and serum response factor as novel target molecules of the cancer-amplified transcription coactivator ASC-2”. Molecular Endocrinology 14 (6): 915–25. (June 2000). doi:10.1210/mend.14.6.0471. PMID 10847592.
- ^ “Steroid receptor coactivator-1 coactivates activating protein-1-mediated transactivations through interaction with the c-Jun and c-Fos subunits”. The Journal of Biological Chemistry 273 (27): 16651–4. (July 1998). doi:10.1074/jbc.273.27.16651. PMID 9642216.
- ^ “Pin1 is overexpressed in breast cancer and cooperates with Ras signaling in increasing the transcriptional activity of c-Jun towards cyclin D1”. The EMBO Journal 20 (13): 3459–72. (July 2001). doi:10.1093/emboj/20.13.3459. PMC 125530. PMID 11432833.
- ^ “Molecular cloning and characterization of CAPER, a novel coactivator of activating protein-1 and estrogen receptors”. The Journal of Biological Chemistry 277 (2): 1229–34. (January 2002). doi:10.1074/jbc.M110417200. PMID 11704680.
- ^ “Recruitment of the retinoblastoma protein to c-Jun enhances transcription activity mediated through the AP-1 binding site”. The Journal of Biological Chemistry 274 (9): 5454–61. (February 1999). doi:10.1074/jbc.274.9.5454. PMID 10026157.
- ^ “Human De-etiolated-1 regulates c-Jun by assembling a CUL4A ubiquitin ligase”. Science 303 (5662): 1371–4. (February 2004). Bibcode: 2004Sci...303.1371W. doi:10.1126/science.1093549. PMID 14739464.
- ^ “Characterization of human constitutive photomorphogenesis protein 1, a RING finger ubiquitin ligase that interacts with Jun transcription factors and modulates their transcriptional activity”. The Journal of Biological Chemistry 278 (22): 19682–90. (May 2003). doi:10.1074/jbc.M212681200. hdl:2434/518351. PMID 12615916.
- ^ a b “AP-1 and Cbfa/runt physically interact and regulate parathyroid hormone-dependent MMP13 expression in osteoblasts through a new osteoblast-specific element 2/AP-1 composite element”. The Journal of Biological Chemistry 276 (23): 20029–38. (June 2001). doi:10.1074/jbc.M010601200. PMID 11274169.
- ^ a b “Physical interaction of the activator protein-1 factors c-Fos and c-Jun with Cbfa1 for collagenase-3 promoter activation”. The Journal of Biological Chemistry 277 (1): 816–22. (January 2002). doi:10.1074/jbc.M107082200. PMID 11641401.
- ^ “Smad3 and Smad4 cooperate with c-Jun/c-Fos to mediate TGF-beta-induced transcription”. Nature 394 (6696): 909–13. (August 1998). Bibcode: 1998Natur.394..909Z. doi:10.1038/29814. PMID 9732876.
- ^ “Tumor necrosis factor-alpha inhibits transforming growth factor-beta /Smad signaling in human dermal fibroblasts via AP-1 activation”. The Journal of Biological Chemistry 275 (39): 30226–31. (September 2000). doi:10.1074/jbc.M005310200. PMID 10903323.
- ^ “Smads bind directly to the Jun family of AP-1 transcription factors”. Proceedings of the National Academy of Sciences of the United States of America 96 (9): 4844–9. (April 1999). Bibcode: 1999PNAS...96.4844L. doi:10.1073/pnas.96.9.4844. PMC 21779. PMID 10220381.
- ^ a b “Interacting regions in Stat3 and c-Jun that participate in cooperative transcriptional activation”. Molecular and Cellular Biology 19 (10): 7138–46. (October 1999). doi:10.1128/MCB.19.10.7138. PMC 84707. PMID 10490649.
- ^ “c-Jun interacts with the corepressor TG-interacting factor (TGIF) to suppress Smad2 transcriptional activity”. Proceedings of the National Academy of Sciences of the United States of America 98 (11): 6198–203. (May 2001). Bibcode: 2001PNAS...98.6198P. doi:10.1073/pnas.101579798. PMC 33445. PMID 11371641.
関連文献
編集- “Human proto-oncogene c-jun encodes a DNA binding protein with structural and functional properties of transcription factor AP-1”. Science 238 (4832): 1386–92. (December 1987). Bibcode: 1987Sci...238.1386B. doi:10.1126/science.2825349. PMID 2825349.
- “Jun: transcription factor and oncoprotein”. Journal of Molecular Medicine 74 (12): 725–47. (December 1996). doi:10.1007/s001090050077. PMID 8974016.
- “Marek's disease herpesvirus transforming protein MEQ: a c-Jun analogue with an alternative life style”. Virus Genes 21 (1–2): 51–64. (2001). doi:10.1023/A:1008132313289. PMID 11022789.
- “[Possible role of transcription factor AP1 in the tissue-specific regulation of human papillomavirus]”. Revista de Investigacion Clinica 54 (3): 231–42. (2002). PMID 12183893.
- “The activator protein-1 transcription factor in respiratory epithelium carcinogenesis”. Molecular Cancer Research 5 (2): 109–20. (February 2007). doi:10.1158/1541-7786.MCR-06-0311. PMID 17314269.
関連項目
編集外部リンク
編集- c-jun Proteins - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス
- c-jun Genes - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス
- Drosophila Jun-related antigen - The Interactive Fly
- FactorBook C-Jun
- Human JUN genome location and JUN gene details page in the UCSC Genome Browser.