亜塩素酸ナトリウム
亜塩素酸ナトリウム(あえんそさん—)は、亜塩素酸のナトリウム塩で、化学式 NaClO2 と表される無機化合物である。毒物及び劇物取締法により劇物に指定されている[1]。また日本の消防法では危険物第1類の酸化性固体に分類される。
| 亜塩素酸ナトリウム | |
|---|---|
| |
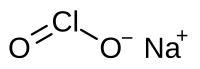
亜塩素酸ナトリウム | |
| 識別情報 | |
| CAS登録番号 | 7758-19-2 |
| KEGG | C19523 |
| RTECS番号 | VZ4800000 |
| 特性 | |
| 化学式 | NaClO2 |
| モル質量 | 90.44 g/mol |
| 外観 | 白色の固体 |
| 匂い | 刺激臭 |
| 密度 | 2.5 g/cm3, 固体 |
| 融点 |
180–200 °C 分解 |
| 水への溶解度 | 39 g/100 ml (17 °C) |
| 危険性 | |
| EU分類 | 記載無し |
| NFPA 704 | |
| 引火点 | 無し |
| 関連する物質 | |
| その他の陰イオン | 塩化ナトリウム 次亜塩素酸ナトリウム 塩素酸ナトリウム 過塩素酸ナトリウム |
| その他の陽イオン | 亜塩素酸カリウム 亜塩素酸バリウム |
| 関連物質 | 二酸化塩素 亜塩素酸 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
合成
編集二酸化塩素に水酸化ナトリウムと過酸化水素とを反応させると、亜塩素酸ナトリウムが得られる(式)。
性質
編集白色の結晶で、水によく溶ける。特異な刺激臭があり、水溶液に塩素(式)、あるいは次亜塩素酸ナトリウムを作用させたり、電気酸化を行うと、二酸化塩素が発生する。
用途
編集また、有機合成化学では、アルデヒドをカルボン酸へ変換する酸化剤として用いられる(式)。この反応の活性種は亜塩素酸 (HClO2) である。
反応は多くの場合、リン酸緩衝液などで pH を微弱な酸性に保った状態で行われる。さらに、系中で発生する次亜塩素酸 (HClO) など、副反応を誘発する塩素化合物を捕捉するために、2-メチル-2-ブテンなどの捕捉剤(スカベンジャー)が添加される。
この反応は、収率や化学選択性が高く、後処理が簡便であるため、カルボン酸の合成法として非常に重要である。1級アルコールをカルボン酸に変換する場合でも、強い酸化剤を用いてアルコールを1段階で直接カルボン酸に変えようとするよりも、スワーン酸化やTPAP酸化によりアルコールをいったんアルデヒドに変え、それから上式の手法でカルボン酸とするほうが、収率や選択性が上回る場合が多い。全合成などで多用される手法である。
