フレカイニド
フレカイニド(Flecainide)はVaughan-Williams分類でIc群に分類される抗不整脈薬である。商品名タンボコール。錠剤と細粒は頻脈性不整脈(心房細動、心房粗動、心室性頻拍)の治療に用いられる。小児にも適応を持ち、発作性上室性頻拍にも用いることができる[1][2]。静注薬はその他「医師が生命に関わると判定した重症の心室性期外収縮」にも使用可能である[3]。フレカイニドは心臓のナトリウムチャネルを遮断して心筋活動電位の延長をもたらす。
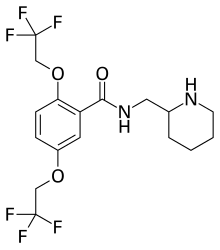 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Tambocor |
| Drugs.com | monograph |
| MedlinePlus | a608040 |
| 胎児危険度分類 |
|
| 薬物動態データ | |
| 生物学的利用能 | 95% |
| 血漿タンパク結合 | 40% |
| 代謝 | CYP2D6 (limited) |
| 半減期 | 20 hours (range 12-27 hours) |
| 排泄 | Renal |
| データベースID | |
| CAS番号 |
54143-55-4 |
| ATCコード | C01BC04 (WHO) |
| PubChem | CID: 3356 |
| IUPHAR/BPS | 2560 |
| DrugBank | DB01195en:Template:drugbankcite |
| ChemSpider |
3239 |
| UNII |
K94FTS1806 |
| KEGG | D07962 en:Template:keggcite |
| ChEBI | CHEBI:75984en:Template:ebicite |
| ChEMBL | CHEMBL652en:Template:ebicite |
| 化学的データ | |
| 化学式 | C17H20F6N2O3 |
| 分子量 | 414.343 g/mol |
| |
効能・効果
編集フレカイニドは刺激伝導系へ作用するので、房室結節回帰性頻拍(AVNRT)やWolff-Parkinson-White症候群(WPW)等の様々な上室性頻拍の治療に使用される。日本での適応は、成人については「頻脈性不整脈(発作性心房細動・粗動、心室性)」、小児については「頻脈性不整脈(発作性心房細動・粗動、発作性上室性、心室性)」である。
心室性頻拍(VT)の一部に用いられる事もある。特に、急性虚血性疾患でない場合に有用である。右心室流出路(RVOT)頻拍の治療[4]や催不整脈性右室異形成(ARVD)[5]の不整脈抑制にも用いられる。臨床試験(中でもCardiac Arrhythmia Suppression Trial)は急性心筋梗塞による期外収縮の抑制にフレカイニドを用いると死亡率が上昇することを示した[6][7]。
ブルガダ症候群の疑い例については、フレカイニドを投与した際の心電図所見(ブルガダ症候群に特徴的な心電図変化(右脚ブロックおよび右側胸部誘導(V1~V3)のST上昇)が顕在化する)が鑑別診断に役立つ場合がある[8]が、この時心室細動、心室頻拍、心室性期外収縮等の発現に注意する必要がある。
フレカイニドは小児の不整脈に対しても使用される。
フレカイニドは心臓のリアノジン受容体からのカルシウム放出を抑制し、マウスおよびヒトでのカテコールアミン誘発多形性心室頻拍の原因を取り除くと考えられている[9]。
用量調節
編集フレカイニドの用量は、患者それぞれの併用薬、疾患併発状態、代謝の影響等により調節すべきである。腎機能障害のある患者では、血中濃度が治療域(中毒域未満)であることを確認する必要がある。加えて、軽度の不整脈に対してはより低用量で使用する事で、副作用の発現頻度を低減させることができる。小児の場合、フレカイニドの用量は体表面積を基に決定する[注 1]。食事がフレカイニドの吸収に影響するので、食事の1時間前に服用させる必要がある。
半減期が延長すると特徴的な心電図のQRS延長が発生し、特に心拍数が多い場合に副作用が発現する[10]。フレカイニドの投与開始や用量変更は、血中濃度が安定するまで(3〜5日間)心電図を観察しながら実施する必要がある。
器質性心疾患のない上室性頻拍、発作性心房細動、心房粗動の治療には50mg×2回/日から投与を開始する。血中濃度が安定した後でも効果が不充分な場合は、100mg×2回/日まで増量できる。
重篤な心室性不整脈(心室性頻拍)の治療には、100mg×2回/日から投与を開始することがある[注 2]。軽度の場合同様、血中濃度が安定するまでは増量すべきでない。
作用機序
編集フレカイニドは心臓のNav1.5ナトリウムチャネルを遮断し、心筋活動電位の持続時間を延長させる[11]。これにより心臓内部の電気刺激の伝達が遅くなり、心筋の興奮性が抑制される。特に刺激伝導系および心室筋細胞において顕著である。心室筋でのフレカイニドの効果は、駆出率の低下に繋がる筋収縮性を減少させる。
心臓のナトリウムチャネルへの効果は心拍数の増加と共に増強される[12]。これは使用依存性または頻度依存性と称され、フレカイニドが徐脈性不整脈の予防よりも頻脈性不整脈の治療に適していることを意味する。
薬物動態学
編集フレカイニドを経口投与した場合の生物学的利用能は高く[13]、吸収された薬物は血流に乗って全身に分布する。最高血中濃度に達するのは投与後1〜6時間である。血中半減期はおよそ20時間であるが個人差が大きく、12〜27時間と開きがある[14]。経口投与を開始してから血中濃度が安定するまでは概ね3-5日を要する。
フレカイニドは主に腎臓から排泄されるほか、肝臓のCYP2D6で代謝される[15]。従って、腎機能の低下や尿pHの変動はフレカイニドの排泄に大きく関係する。
排出経路が2つある事と心筋の収縮性を減少させる性質のため[16]、フレカイニドは多くの医薬品と相互作用し、心筋抑制薬や房室結節抑制薬の効果に影響を与える。加えて、フレカイニドはシトクロムP450で代謝される薬剤の多く(全てではない)に影響する。
日本の添付文書で併用禁忌・併用注意とされている薬剤を下記に挙げる。
併用禁忌
編集併用注意
編集副作用
編集重大な副作用として添付文書に記載されているものは、心室頻拍、トルサード・ド・ポワント、心室細動、心房粗動、高度房室ブロック、一過性心停止、洞停止または洞房ブロック、心不全悪化、アダムス・ストークス発作、肝機能障害、黄疸である。
臨床試験Cardiac Arrhythmia Suppression Trial(CAST)の結果、器質性心疾患(心筋梗塞、左室不全等)のある患者や心室性不整脈のある患者はフレカイニドを用いるべきではないとされた。この結果は有意で、臨床試験が中止され、中間解析結果が公表された[17]。これらの疾患を有する患者では、フレカイニド投与により致死性不整脈の発現頻度が上昇する。
投与量は臨床計画に添って調整すべきである。他の全ての抗不整脈薬にはフレカイニドとの併用による催不整脈作用がある。特に他のIc群抗不整脈薬と併用した場合にリスクが増大する。催不整脈リスクは低カリウム血症でも増加する[18]。フレカイニドの投与期間にはよらず、遅発性の不整脈も報告されている[19]。フレカイニド排泄に腎臓および肝臓の両方が関わっているため、腎機能障害または肝機能障害がある場合には個別に投与量を調節する必要がある。
フレカイニドに陰性変力作用[16]があるため、駆出率が低下している患者や心不全のある患者に用いる場合には注意が必要である。虚血性心疾患のある患者や高齢者には用いるべきでない。
他のI群の抗不整脈薬同様、フレカイニドは心臓ペースメーカーの動作閾値を上昇させる[20]。そのため、フレカイニドの血中濃度が安定した後に、ペースメーカーを再調整する必要がある。
心毒性
編集フレカイニドの治療指数が狭い[注 3]ので、トルサード・ド・ポワントの様な致死的毒性の兆候に常に注意を払う必要がある。フレカイニドの毒性は血中濃度と密接に関連している[21]が、患者一人一人の血中濃度を日常診療で把握しておく事は不可能に近い。
フレカイニドの毒性の兆候は心電図上のPR延長およびQRS延長として現れる。心筋収縮力の突然の低下による心不全の顕在化の症状である可能性がある。
心毒性の治療
編集フレカイニドの心毒性の治療方針は、フレカイニドの排泄促進、フレカイニドの心作用遮断、および(稀に、致死的不整脈が差し迫っている場合の)補助人工心臓の利用の3つである。β作動薬投与[21]やナトリウム負荷[21](一般に高濃度炭酸水素ナトリウム)は実績がある。人工心肺に繋いで心臓の負荷を低減し、肝臓への血流量を確保した例もある[22][23]。
肺毒性
編集フレカイニドは肺に対して非常に親和性が高く[24]、薬剤性間質性肺炎の原因となり得る[25][26][27][28][29]。
長期投与
編集注釈
編集出典
編集- ^ “タンボコール錠50mg/ タンボコール錠100mg 添付文書” (2012年9月). 2016年6月29日閲覧。
- ^ “タンボコール細粒10% 添付文書” (2015年6月). 2016年6月29日閲覧。
- ^ “タンボコール静注50mg 添付文書” (2012年9月). 2016年6月29日閲覧。
- ^ Gill J, Mehta D, Ward D, Camm A (1992). “Efficacy of flecainide, sotalol, and verapamil in the treatment of right ventricular tachycardia in patients without overt cardiac abnormality”. Br Heart J 68 (4): 392–7. doi:10.1136/hrt.68.10.392. PMC 1025139. PMID 1449923.
- ^ Sakurada H, Hiyoshi Y, Tejima T, Yanase O, Tokuyasu Y, Watanabe K, Motomiya T, Sugiura M, Hiraoka M (1990). “[Effects of oral flecainide treatment of refractory tachyarrhythmias]”. Kokyu to Junkan 38 (5): 471–6. PMID 2115193.
- ^ Echt D, Liebson P, Mitchell L, Peters R, Obias-Manno D, Barker A, Arensberg D, Baker A, Friedman L, Greene H (1991). “Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial”. N Engl J Med 324 (12): 781–8. doi:10.1056/NEJM199103213241201. PMID 1900101.
- ^ Greenberg H, Dwyer E, Hochman J, Steinberg J, Echt D, Peters R (1995). “Interaction of ischaemia and encainide/flecainide treatment: a proposed mechanism for the increased mortality in CAST I”. Br Heart J 74 (6): 631–5. doi:10.1136/hrt.74.6.631. PMC 484119. PMID 8541168.
- ^ Gasparini M, Priori S, Mantica M, Napolitano C, Galimberti P, Ceriotti C, Simonini S (2003). “Flecainide test in Brugada syndrome: a reproducible but risky tool”. Pacing Clin Electrophysiol 26 (1 Pt 2): 338–41. doi:10.1046/j.1460-9592.2003.00045.x. PMID 12687841.
- ^ Watanabe, Hiroshi; Nagesh Chopra; Derek Laver; Hyun Seok Hwang; Sean S. Davies; Daniel E. Roach; Henry J. Duff; Dan M. Roden et al. (2009-04-01). “Flecainide prevents catecholaminergic polymorphic ventricular tachycardia (CPVT) in mice and humans.”. Nature Medicine 15 (4): 380–383. doi:10.1038/nm.1942. PMC 2904954. PMID 19330009 2009年5月4日閲覧。.
- ^ Katristis D, Rowland E, O'Nunain S, Shakespeare C, Poloniecki J, Camm A (1995). “Effect of flecainide on atrial and ventricular refractoriness and conduction in patients with normal left ventricle Implications for possible antiarrhythmic and proarrhythmic mechanisms”. Eu Heart J 16 (1): 1930–1935. PMID 8682029.
- ^ Ramos E, O'leary M (2004). “State-dependent trapping of flecainide in the cardiac sodium channel”. J Physiol 560 (Pt 1): 37–49. doi:10.1113/jphysiol.2004.065003. PMC 1665201. PMID 15272045.
- ^ Wang Z, Fermini B, Nattel S (1993). “Mechanism of flecainide's rate-dependent actions on action potential duration in canine atrial tissue”. J Pharmacol Exp Ther 267 (2): 575–81. PMID 8246130.
- ^ Smith G (1985). “Flecainide: a new class Ic antidysrhythmic”. Drug Intell Clin Pharm 19 (10): 703–7. PMID 3902429.
- ^ Padrini R, Piovan D, Busa M, al-Bunni M, Maiolino P, Ferrari M (1993). “Pharmacodynamic variability of flecainide assessed by QRS changes”. Clin Pharmacol Ther 53 (1): 59–64. doi:10.1038/clpt.1993.9. PMID 8422742.
- ^ Haefeli W, Bargetzi M, Follath F, Meyer U (1990). “Potent inhibition of cytochrome P450IID6 (debrisoquin 4-hydroxylase) by flecainide in vitro and in vivo”. J Cardiovasc Pharmacol 15 (5): 776–9. doi:10.1097/00005344-199005000-00013. PMID 1692938.
- ^ a b Santinelli V, Arnese M, Oppo I, Matarazzi C, Maione S, Palma M, Giunta A (1993). “Effects of flecainide and propafenone on systolic performance in subjects with normal cardiac function”. Chest 103 (4): 1068–73. doi:10.1378/chest.103.4.1068. PMID 8131440.
- ^ Cardiac Arrhythmia Suppression Trial (CAST) Investigators (1989). “Preliminary report: effect of encainide and flecainide on mortality in a randomized trial of arrhythmia suppression after myocardial infarction.”. N Engl J Med. 321 (6): 406–412. doi:10.1056/NEJM198908103210629. PMID 2473403.
- ^ Ohki R, Takahashi M, Mizuno O, Fujikawa H, Mitsuhashi T, Katsuki T, Ikeda U, Shimada K (2001). “Torsades de pointes ventricular tachycardia induced by mosapride and flecainide in the presence of hypokalemia”. Pacing Clin Electrophysiol 24 (1): 119–21. doi:10.1046/j.1460-9592.2001.00119.x. PMID 11227957.
- ^ Morganroth J (1992). “Early and late proarrhythmia from antiarrhythmic drug therapy”. Cardiovasc Drugs Ther 6 (1): 11–4. doi:10.1007/BF00050910. PMID 1533532.
- ^ Fornieles-Pérez H, Montoya-García M, Levine P, Sanz O (2002). “Documentation of acute rise in ventricular capture thresholds associated with flecainide acetate”. Pacing Clin Electrophysiol 25 (5): 871–2. doi:10.1046/j.1460-9592.2002.00871.x. PMID 12049386.
- ^ a b c Winkelmann B, Leinberger H (1987). “Life-threatening flecainide toxicity. A pharmacodynamic approach”. Annals of Internal Medicine 106 (6): 807–14. doi:10.7326/0003-4819-106-6-807. PMID 3107447.
- ^ Corkeron M, van Heerden P, Newman S, Dusci L (1999). “Extracorporeal circulatory support in near-fatal flecainide overdose”. Anaesth Intensive Care 27 (4): 405–8. PMID 10470398.
- ^ Yasui R, Culclasure T, Kaufman D, Freed C (1997). “Flecainide overdose: is cardiopulmonary support the treatment?”. Annals of Emergency Medicine 29 (5): 680–2. doi:10.1016/S0196-0644(97)70257-9. PMID 9140253.
- ^ Latini R, Cavalli A, Maggioni AP, Volpi A (December 1987). Flecainide distribution in human tissues. 24. pp. 820–2. PMC 1386410. PMID 3125854.
- ^ Ozkan M, Dweik RA, Ahmad M (September 2001). Drug-induced lung disease. 68. pp. 782–5, 789–95. PMID 11563482.
- ^ P Camus, A Fanton, P Bonniaud, C Camus et al. "Interstitial lung disease induced by drugs and radiation. Respiration 2004; 71:301–326 doi:10.1159/000079633 PMID 15316202
- ^ S Pesenti, D Lauque, G Daste, V Boulay et al. "Diffuse Infiltrative Lung Disease Associated with Flecainide. Respiration 2002; 69:182–185 doi:10.1159/000056325 PMID 11961436
- ^ Haas M, Pérault MC, Bonnefoy P, Rodeau F, Caron F (2001). [Interstitial pneumopathy due to flecainide]. 30. pp. 1062. PMID 11471279.
- ^ Robain A, Perchet H, Fuhrman C (February 2000). Flecainide-associated pneumonitis with acute respiratory failure in a patient with the LEOPARD syndrome. 55. pp. 45–7. PMID 10707759.
- ^ Aliot E, Capucci A, Crijns HJ, Goette A, Tamargo J. Twenty-five years in the making: flecainide is safe and effective for the management of atrial fibrillation. Eurospace 2011 13:161-173