リボヌクレアーゼA
リボヌクレアーゼA(Ribonuclease A)は、一本鎖RNAを切断するエンドヌクレアーゼの1つである。RNAアーゼA(RNase A)とも言う。子牛の膵臓のRNAアーゼAは、古典的なタンパク質科学のモデル系として用いられた。
歴史
編集子牛の膵臓由来のRNAアーゼAは、アメリカ合衆国の食肉会社Armour and Companyがkg単位で精製し、興味のある科学者に10mgずつ無料で提供したことから広く使われるようになった。この入手の利便性によって、RNAアーゼはタンパク質研究のモデルとなった。
RNAアーゼは研究の素材として、吸光、円偏光二色性、旋光分散、ラマン分光法、電子スピン共鳴、核磁気共鳴分光法など様々な分光学的分析手法を生み出した。また限定分解、側鎖の化学修飾、抗原認識などいくつかの化学的構造分析法の発展にも貢献した。
1967年にはタンパク質として3番目に構造が解かれている[1]。
RNAアーゼAの酸化的フォールディングの研究から、クリスチャン・アンフィンセンはタンパク質のフォールディングに関して熱動力学仮説を立て、タンパク質のフォールドは自由エネルギーが最小になるように決まるとした。
さらに、RNAアーゼAはマルチプルアライメントによる解析が初めて行われたタンパク質、進化的な特徴が比較された初めてのタンパク質でもある。
構造と特徴
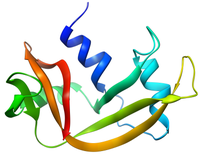
編集RNAアーゼAは124残基、13.7kDa以下と比較的小さいタンパク質である。2層のα+βからなり、タコスのように2つに折り畳まれて、中央の溝がRNA結合部位になる。N末端側の1番目の層は3つのαヘリックスからなり、C末端側の2番目の層は2つのβシート中に2つのβヘアピンが配置した構造からなっている。
RNAアーゼAは、Cys26-Cys84、Cys58-110、Cys40-95、Cys65-72という4つのジスルフィド結合を持つ。最初の2つはフォールディングに必須で、それぞれが第1層のαヘリックスと第2層のβシートを結合して疎水中心を作っている。後の2つはフォールディングには必須ではなく、どちらかを欠いても構造は変わらない。これらはループをつなげて溶媒に露出させる。興味深いことに、最後のジスルフィド結合はループのエントロピーに比べて結合を非常に形成しやすい。これはこの部分のβヘアピンの形成しやすさを反映していると考えられる。
RNAアーゼAは等電点が約8.63の塩基性のタンパク質であり、多数の陽電荷がRNAとの結合に関与する。さらに一般的に言うと、RNAアーゼは非常に極性が大きく、疎水性基が少ない。このため、構造の安定化のために4つものジスルフィド結合が必要となる。
酵素としての機能
編集RNAアーゼAの陽電荷は主に溝の周りに分布している。RNA分子が溝の位置に来ると2つのヒスチジンHis12とHis119によって切断される。中間体は近辺にある3つのリシンLys7、Lys41、Lys66によって安定化される。
抗がん作用
編集RNAアーゼAやそのオリゴマー、ホモログは、特にガン細胞に対しての細胞毒性、細胞増殖抑制の作用を持っている。この効果を使って、RNAアーゼのホモログであるオンコナーゼからリボヌクレアーゼ薬剤が作られ、特に皮膚がんの外用薬として用いられている。
その他の生理活性
編集出典
編集- ^ Wyckoff HW, Hardman KD, Allewell NM, Inagami T, Johnson LN, Richards FM. The structure of ribonuclease-S at 3.5 A resolution. J Biol Chem. 1967 Sep 10;242(17):3984-8. PMID 6037556
- D'Alessio G and Riordan JF, eds. (1997) Ribonucleases: Structures and Functions, Academic Press.
- Raines RT. (1998) "Ribonuclease A", Chem. Rev., '98, 1045-1065.
- Scheraga HA, Wedemeyer WJ and Welker E. (2001) "Bovine Pancreatic Ribonuclease A: Oxidative and Conformational Folding Studies", Methods Enzymol., 341, 189-221.