チオ硫酸
チオ硫酸(チオりゅうさん、英語: thiosulfuric acid)とは、硫黄のオキソ酸の一種で、化学式 H2S2O3 の化合物。本稿ではチオ硫酸とその塩ならびにイオンについて述べる。
| チオ硫酸[1] | |
|---|---|

| |
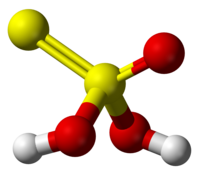
| |
sulfurothioic O-acid | |
別称 チオ硫酸 | |
| 識別情報 | |
| CAS登録番号 | 13686-28-7 |
| PubChem | 24478 |
| ChemSpider | 22886 |
| |
| |
| 特性[1][2] | |
| 化学式 | H2S2O3 |
| モル質量 | 114.14 g/mol |
| 融点 |
0 °C以下で分解 |
| 水への溶解度 | 分解 |
| 酸解離定数 pKa | 0.6, 1.74 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
チオ硫酸は酸解離定数がpKa1 = 0.6、pKa2 = 1.6の二価の無機酸である[3][4]。その塩であるチオ硫酸塩は次亜硫酸塩と誤まって呼ばれることがある[5]。
性質
編集チオ硫酸塩のアンモニア、アルカリ金属塩、アルカリ土類金属塩は水溶性が大であり、中性ないしはアルカリ性水溶液は比較的安定である。一方、強酸性水溶液中では不均化によりコロイド状硫黄と二酸化硫黄とに分解するので水溶液から遊離させることは困難である。遊離のチオ硫酸は低温下でジエチルエーテル錯体として単離された例や液体二酸化炭素中で単離された例が知られている。生成した遊離酸は不安定で低温でも硫化水素と三酸化硫黄に分解するが高温ではさらに分解が進み硫黄、二酸化硫黄、水が生成する。空気中では水とも酸素とも反応するので生成物は複雑であり前述の分解生成物に加えて、硫化水素、ポリ硫化水素、硫酸、ポリチオン酸なども生成する。[5][6]
チオ硫酸塩
編集チオ硫酸イオンは4面体構造をとり、硫黄原子は中心と1つの頂点に、酸素原子は他の頂点に配置する。この様にチオ硫酸の二つの原子は等価ではなく頂点に位置する硫黄は酸化還元能や錯体形成能などチオ硫酸塩の化学的性質を特徴づけている[5][6]。
酸化還元剤としては単体ハロゲンの還元に利用される。すなわち、反応が定量的に進行しチオ硫酸イオンは硫酸イオンとなるためヨウ素滴定の滴定試薬として利用される。他に定量的に酸化還元反応が進行するものとして、塩素、臭素、過マンガン酸塩、クロム酸塩などがあげられる。日用品としては水道水中の残留塩素を無毒化したりする用途で、鑑賞用魚類の水質改善剤や塩素除去用の食品添加物としてしばしば利用される。[5][7][6]
上記以外にもチオ硫酸塩はさまざまな酸化還元反応を示す。酸性溶液中の過酸化水素に対しては四チオン酸塩ないしは三チオン酸塩を生成するのに対してアルカリ性の過酸化水素に対しては硫酸イオンを生成する。あるいは金属を酸化することで銅、亜鉛、アルミニウムを腐食し硫化物を生成する。[6]
キレート剤としては、写真の定着プロセスに利用して現像しなかった難溶性のハロゲン化銀を過剰量のチオ硫酸塩で処理することで銀のチオスルファト錯体として可溶化する。この性質は金(I)塩、銀(I)塩、銅(I)塩で共通する性質である。[7][6]
製法
編集チオ硫酸塩の工業的製法は原料により分類すると以下の三つが知られている[6]。
- 中性またはアルカリ性条件下で単体硫黄と亜硫酸塩とを反応させる方法
- 中性またはアルカリ性条件下で多硫化物と亜硫酸塩とを反応させる方法
- 硫化物塩に対して二酸化硫黄、亜硫酸塩、亜硫酸水素塩を反応させる方法
利用
編集チオ硫酸イオン自体の毒性は低く、無水チオ硫酸ナトリウムのLD50(ラット)は約7.5 g/kg(経路不明)ないしは約2.5g/kg(静脈内投与)。LD50(イヌ)は約3 g/kg(静脈内投与)である。低毒性とチオ硫酸イオンのキレート能力から重金属(水銀、銅、鉛等)の解毒薬として利用されたり、ヒ素やシアン化水素との反応性からこれらの物質の中毒に対して解毒剤として使用する例がある。[8][6]
硫黄細菌の一部はチオ硫酸塩を硫黄に転換することでエネルギー代謝の酸化物として利用している。[9]
チオ硫酸塩は低毒性であるが、富栄養化などなど水質を悪化させる要因ともなるので、次亜塩素酸ナトリウムなどで酸化分解してから環境放出することが望ましい[8]。
以下のチオ硫酸塩はいずれも安定である。
- チオ硫酸アンモニウム
- チオ硫酸カリウム
- チオ硫酸カルシウム
- チオ硫酸ナトリウム — 通称ハイポ
出典
編集- ^ a b Macintyre, Jane Elizabeth titys, ed. (1992), Dictionary of Inorganic Compounds, Chapman & Hall, p. 3362, ISBN 0412301202
- ^ Page, F. M. (1953), “The dissociation constants of thiosulphuric acid”, J. Chem. Soc.: 1719–24, doi:10.1039/JR9530001719
- ^ 長倉三郎ら編、「チオ硫酸」、『岩波理化学辞典』、第5版CD-ROM版、岩波書店、1999年。ISBN 4-00-130102-4
- ^ 「無機酸の酸解離定数」、『化学便覧』、改訂5版 基礎編、丸善。ISBN 978-4621073414
- ^ a b c d 長倉三郎ら編、「チオ硫酸塩」、『岩波理化学辞典』、第5版CD-ROM版、岩波書店、1999年。ISBN 4-00-130102-4
- ^ a b c d e f g J.W.Swain, Jr.、「チオ硫酸塩」、『カーク・オスマー化学大辞典』 ISBN 978-4621032923
- ^ a b 長倉三郎ら編、「チオ硫酸ナトリウム」、『岩波理化学辞典』、第5版CD-ROM版、岩波書店、1999年。ISBN 4-00-130102-4
- ^ a b チオ硫酸ナトリウム MSDS
- ^ 八杉龍一ら編、「硫黄細菌」、『岩波生物学辞典』、第4版CD-ROM版、岩波書店、1998年。ISBN 4-00-130070-2