シラン (化合物)
シラン(英: silane)とはケイ素の水素化物で化学式SiH4、分子量32.12の無機化合物である。水素化ケイ素(すいそかケイそ)とも呼ばれる。特異な臭気を有する無色の気体であり、液化ガスとして入手が可能である。
| シラン (化合物) | |
|---|---|
|

|
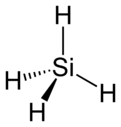
Silane | |
別称 Monosilane Silicane | |
| 識別情報 | |
| CAS登録番号 | 7803-62-5 |
| PubChem | 23953 |
| ChemSpider | 22393 |
| J-GLOBAL ID | 200907042924457559 |
| EC番号 | 232-263-4 |
| 国連/北米番号 | 2203 |
| ChEBI | |
| RTECS番号 | VV1400000 |
| Gmelin参照 | 273 |
| |
| |
| 特性 | |
| 化学式 | H4Si |
| モル質量 | 32.12 g mol−1 |
| 精密質量 | 32.008226661 g mol-1 |
| 外観 | 無色の気体 |
| 密度 | 1.342 g dm-3 |
| 融点 |
−185 °C, 88 K, -301 °F |
| 沸点 |
−112 °C, 161 K, -170 °F |
| 水への溶解度 | ゆっくりと反応する |
| 構造 | |
| 分子の形 | 四面体形
r(Si-H) = 1.4798 angstroms |
| 双極子モーメント | 0 D |
| 熱化学 | |
| 標準生成熱 ΔfH |
34.31kJ/mol |
| 標準モルエントロピー S |
204.6 J mol-1 K-1 |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 0564 |
| EU Index | Not listed |
| 主な危険性 | 非常に強い可燃性、自然発火性 |
| NFPA 704 | |
| 引火点 | きわめて引火性が高い気体 |
| 発火点 | 294 K (21 °C) (~70 °F) |
| 爆発限界 | 1.37–100% |
| 許容曝露限界 | 5 ppm (ACGIH TLV) |
| 関連する物質 | |
| 関連するモノシラン類 | フェニルシラン |
| 関連物質 | メタン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ケイ素数2、3の高級水素化物はそれぞれジシラン、トリシランと呼ばれ、それと区別するためにSiH4はモノシランとも呼ばれる。
概要
編集空気中の酸素によりすみやかに酸化されて水と二酸化ケイ素に分解し、シランの濃度が高ければ着火源がなくても自発的に発火燃焼する。燃焼に伴い、二酸化ケイ素のフュームが発生するので吸い込まないように注意が必要である。また、刺激性が強く、吸引すると肺気腫を引き起こす恐れがある。
シラン中の水素原子はケイ素を中心とした正四面体の各頂点に位置している。アルカン同様に極性が小さく、ヘキサン、エーテルなどの有機溶媒によく溶ける。アルコール類とはゆっくりと反応する。もっとも単純な気体状のケイ素化合物であり、半導体製造に用いられる特殊材料ガスの代表である。
性質
編集シランはメタンのケイ素アナログである。ケイ素と比較して水素の電気陰性度が大きいため、このSi–H結合の極性はメタンのC–H結合の極性と逆である。この逆転した極性の一つの帰結として、シランは遷移金属と錯体を形成しやすい。2つ目の帰結は、シランが自然発火性ということである。すなわち、シランは外部点火を必要とせずに、空気中で自然発火する[1]。しかしながら、入手できる(しばしば相反する)燃焼データを説明するのが困難なのは、シラン自身は安定であることや、生産の間により大きなシランが自然に形成されるという事実のせいであり、湿気といった不純物や容器表面の触媒効果に対する燃焼の影響の受けやすさがその自然発火性の原因となる[2][3]。420 ℃以上で、シランはケイ素と水素へ分解する。したがって、シリコンの化学蒸着に使うことができる。
Si–H結合の強さは約384 kJ/molであり、H2中のH–H結合よりも約20% 弱い。その結果として、Si-H結合を含む化合物はH2よりも反応性が高い。Si–H結合の強さはその他の置換基によって多少は影響を受ける。SiHF3、SiHCl3、SiHMe3中のSi–H結合の強さはそれぞれ419、382、398 kJ/molである[4][5]。
危険性
編集シランは空気中で自然発火し水、ハロゲンと反応するため大変危険である。
とはいえ、大量の水で冷却、消火することもあるが、ハロゲン系消火剤の使用は禁忌である。[7]二酸化炭素、粉末消火剤を使うと良い。
1991年大阪大学シランガス爆発事故では酸化剤である亜酸化窒素が逆止弁のOリングを腐食、シランガスボンベに逆流引火し結果2名死亡、5名負傷の惨事となった。[8]以降特定高圧ガスに指定され数量によらず届け出が必要である。[9]
製法
編集実験室レベルの製法では、ケイ化マグネシウムと塩酸ないし塩化アンモニウムの反応で生じる。現在ではこの方法は副生物ジシランを目的として使われる程度である。他ケイ素、水素を原料とする不均化反応法があり[6]、工業的生産ではこちらがもっぱら用いられる。
ポリシラン
編集一般式SinH2n+2 (n > 2) の化合物の総称。ケイ素数が規定できるものはオリゴシランと呼ばれることもある。性質はケイ素を炭素に置換したアルカンとはかなり異なり、低い最低遷移エネルギーを持つなどの興味深い性質を示す。一般にはケイ素−ケイ素結合を構築する反応としてはハロシランのアルカリ金属によるウルツ型カップリングのみが採用されるため、アルカンに比べると化合物の多彩さに欠く。
母体の水素置換体は空気中の酸素により爆発的に酸化され、自発的な燃焼を伴うので取り扱いが困難であることから、ケイ素上にアルキルもしくはアリール基を有する誘導体の研究が多い。特殊高圧ガスである。
有機シラン
編集現在までに多くのシラン誘導体が合成されている。メチル化物であるテトラメチルシランは、核磁気共鳴分光法におけるプロトン、炭素13、およびケイ素29の核種の標準物質として用いられる。有機化学ではそれらの一般式がRR1R2R3Si(各置換基はHまたは有機基)と表される誘導体の総称を指してシランと呼ぶことが多い。詳細は項目: 有機ケイ素化合物 を参照のこと。
脚注
編集- ^ Emeléus, H. J. & Stewart, K. (1935). “The oxidation of the silicon hydrides”. Journal of the Chemical Society: 1182–1189. doi:10.1039/JR9350001182.
- ^ Koda, S. (1992). “Kinetic Aspects of Oxidation and Combustion of Silane and Related Compounds”. Progress in Energy and Combustion Science 18 (6): 513–528. doi:10.1016/0360-1285(92)90037-2.
- ^ Timms, P. L. (1999). “The chemistry of volatile waste from silicon wafer processing”. Journal of the Chemical Society – Dalton Transactions (6): 815–822. doi:10.1039/a806743k.
- ^ M. A. Brook "Silicon in Organic, Organometallic, and Polymer Chemistry" 2000, J. Wiley, New York. ISBN 0-471-19658-4.
- ^ “Bond Energies”. Michigan State University Organic Chemistry. 2016年11月12日時点のオリジナルよりアーカイブ。2017年6月15日閲覧。
- ^ a b 野中勲,加藤芳久 (1983). “シランの物性と安全な取扱い”. 安全工学 22 (3): 163–168. doi:10.18943/safety.22.3_163.
- ^ “職場のあんぜんサイト:化学物質:シラン”. anzeninfo.mhlw.go.jp. 2023年2月14日閲覧。
- ^ “1991年大阪大学モノシランガス爆発事故”. 川口液化ケミカル株式会社. 2023年2月14日閲覧。
- ^ “シラン Silane | Chem-Station (ケムステ)”. www.chem-station.com. 2023年2月14日閲覧。
- ^ “不安定化合物ヒドロシランをうまくつくる方法 | Chem-Station (ケムステ)”. www.chem-station.com. 2023年2月14日閲覧。
関連項目
編集外部リンク
編集- organofunctional silanes from Degussa AG
- organofunctional silanes for building protection - water repellents - masonry protection - Graffiti Controll - sealer - easy to clean surface from Degussa AG
- http://www.siridion.com/ chlorosilanes for telecommunication and electronic materials from Degussa
- シラン Silane - Chem-Station
- モノシランガスの燃焼実験 - YouTube
- Silane (chemical compound) - ブリタニカ百科事典
