シクロオキシゲナーゼ2
シクロオキシゲナーゼ2(英: cyclooxygenase-2、略称: COX-2)またはプロスタグランジンエンドペルオキシドシンターゼ2(英: prostaglandin-endoperoxide synthase 2、略称: PTGS2)は、ヒトではPTGS2遺伝子にコードされる酵素である[5]。COX-2はヒトに2種類存在するシクロオキシゲナーゼのうちの1つである。COX-2はアラキドン酸からプロスタグランジンH2への変換に関与しており、炎症時に発現する。プロスタグランジンH2はプロスタサイクリンの重要な前駆体である。
機能
編集COX-2(PTGS2)は、アラキドン酸をプロスタグランジンH2(PGH2)に変換する。COXはNSAIDの標的であり、COX-2特異的阻害薬はコキシブ(coxib)と呼ばれる。COX-2は二量体を形成し、各単量体にはペルオキシダーゼとシクロオキシゲナーゼの活性部位が存在する。COXはアラキドン酸からプロスタグランジンへの変換を2段階で触媒する。まず、アラキドン酸の13位の炭素から水素が引き抜かれ、その後2分子の酸素が付加されてプロスタグランジンG2(PGG2)が形成される。続いて、PGG2はペルオキシダーゼ活性部位でPGH2に還元される。合成されたPGH2は組織特異的イソメラーゼによって、プロスタグランジン(PGD2、PGE2、PGF2α)、プロスタサイクリン(PGI2)またはトロンボキサンA2へ変換される[6]。
COX-2はアラキドン酸を主にPGG2へ代謝するが、少量は15-ヒドロキシエイコサテトラエン酸(15-HETE)のラセミ混合物へも変換される。この混合物は、約22%が15(R)-HETE、約78%が15(S)-HETEであり、11(R)-HETEも少量含まれる[7]。2つの15-HETE立体異性体自体にも生物学的活性は存在するが、リポキシンへの代謝がおそらくより重要性が高いものである。アスピリン処理されたCOX-2はアラキドン酸をほぼ15(R)-HETEのみに代謝し、代謝産物はさらにエピリポキシン(epi-lipoxin)へと代謝される[8]。
機構
編集触媒過程では、ペルオキシダーゼ活性とシクロオキシゲナーゼ活性の双方がmechanism-based inhibitionによって不活性化される。このことは、基質が十分に存在する場合でも、ペルオキシダーゼ活性とシクロオキシゲナーゼ活性の双方が1–2分以内に0にまで低下することを意味する[11][12][13]。
アラキドン酸からPGG2への変換は、多価不飽和脂肪酸の自動酸化に類似した一連のラジカル反応であることが示されている[14]。13-pro(S)水素が引き抜かれ、二原子酸素が11位の炭素のペンタジエニルラジカルを捕捉する。11-ペルオキシラジカルは9位の炭素と環化し、8位の炭素で形成された炭素中心ラジカルが12位の炭素と環化し、エンドペルオキシドが形成される。形成されたアリルラジカルは15位の炭素で二原子酸素に捕捉されて15-(S)-ペルオキシルラジカルとなり、その後このラジカルはPGG2に還元される。この反応は以下の証拠によって裏付けられている。(1) 13-pro(S)-水素の引き抜きには大きな速度論的同位体効果が観察される。(2) 触媒の際に炭素中心ラジカルが捕捉される[15]。(3) 13位と15位のアリルラジカル中間体が酸素に捕捉されることで少量の酸化生成物が形成される[16][17]。
13-pro(S)水素が脱プロトン化され、カルバニオンが酸化されてラジカルになるという別の機構も理論的には可能である。しかし、10,10-ジフルオロアラキドン酸の酸素化による11-(S)-ヒドロキシエイコサ-5,8,12,14-テトラエン酸の生成は、フッ素が脱離して共役ジエンが形成されるカルバニオン中間体の生成とは一致しない[18]。また、10,10-ジフルオロアラキドン酸に由来するエンドペルオキシドを含む生成物が存在しないことから、PGG2の合成におけるC-10カルボカチオンの重要性が示唆されていると考えられている[19]。しかし、カチオン性機構では、エンドペルオキシドの生成が13-pro(S)水素の脱離よりも先に起こることが必要である。このことは、アラキドン酸の酸素化の同位体実験の結果と一致しない[20]。
構造
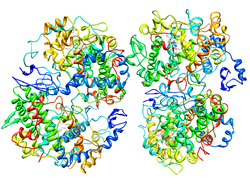
編集COX-2はホモ二量体として存在し、各単量体は約70 kDaである。COX-1(PTGS1)とCOX-2(PTGS2)の三次・四次構造はほぼ同一である。各サブユニットには、N末端の短いEGFドメイン、αヘリカル膜結合領域、C末端の触媒ドメインという3つの構造ドメインが存在する。COXはモノトピック膜タンパク質である。膜結合ドメインは両親媒性のαヘリックスからなり、いくつかの疎水性アミノ酸が膜の単分子層へ露出している。COX-1とCOX-2は二機能酵素であり、空間的には異なる位置にあるが機械的に共役した2つの活性部位で2つの化学反応を連続的に行う。触媒ドメインにはシクロオキシゲナーゼ(COX)活性部位とペルオキシダーゼ活性部位の双方が位置し、タンパク質の約80%を占める。触媒ドメインは、ミエロペルオキシダーゼなどの哺乳類のペルオキシダーゼと相同である[22][23]。
ヒトのCOX-2は触媒単量体(Ecat)とアロステリック単量体(Eallo)という、コンフォメーションの異なる単量体からなる二量体として機能することが判明している。ヘムはEcatのペルオキシダーゼ部位にのみ結合し、EcatのCOX部位は基質や特定の阻害剤(セレコキシブなど)が結合する。EalloのCOX部位には基質と基質以外の脂肪酸(FA)と一部の阻害剤(ナプロキセンなど)が選択的に結合する。アラキドン酸(AA)はEcatとEalloに結合することができるが、Ealloに対するAAの親和性はEcatよりも25倍高い。COX-2の効果的な促進因子であるパルミチン酸はEalloにのみ結合することがマウスのCOX-2とパルミチン酸の共結晶構造から示されている。基質以外の脂肪酸は、脂肪酸の種類や、阻害剤がEcatとEalloのどちらに結合するかに依存して、COX阻害剤の効果は増強されたり減弱されたりする。COX-2が機能する細胞内環境の遊離脂肪酸プールの濃度と組成(FA toneとも呼ばれる)が、COX-2の活性とCOX阻害剤への応答を調節する重要な因子であることが示唆されている[21]。
臨床的意義
編集COX-2は正常条件下では大部分の細胞では発現しておらず、炎症時に発現が上昇することが知られている。COX-1は多くの組織で構成的に発現しており、胃粘膜と腎臓における主要なCOXである。非ステロイド性抗炎症薬(NSAID)は、COX-1とCOX-2によるプロスタグランジンの産生を阻害する。COX-1の阻害は胃で細胞保護作用を有するPGE2やPGI2の基底レベルの産生を低下させ、胃潰瘍に寄与している可能性がある。COX-2は一般的にプロスタグランジンがアップレギュレーションされている細胞(炎症時など)でのみ発現するため、COX-2を選択的に阻害する薬剤候補ではこうした副作用は少ないと考えられているが[23]、一方で心不全、心筋梗塞、脳卒中などの心血管イベントを引き起こす可能性がある[24]。
低用量のアスピリンはCOX-1を遮断してトロンボキサンA2と呼ばれるプロスタグランジンの形成を防ぐことで、心臓発作や脳卒中から保護する。トロンボキサンA2は血小板を凝集させ、血液凝固を促進する。一方、COX-2選択的阻害薬(コキシブ)は心血管イベントを引き起こす可能性がある。ヒトの薬理学や遺伝学、遺伝子操作された齧歯類や他の動物モデル、ランダム化試験での研究からは、COX-2選択的阻害薬によって引き起こされる心血管イベントは、COX-2依存的に心臓を保護するプロスタグランジン、特にプロスタサイクリンの抑制によるものであることが示唆されている。COX-2は血管内壁に存在するプロスタサイクリンのより重要な産生源であり、プロスタサイクリンは血小板の凝集を防ぐため、血液凝固による心血管イベントのリスクが増加する[24][25]。
COX-2の発現は多くのがんでアップレギュレーションされている。COX-2の過剰発現は、血管新生やSLC2A1(GLUT1)の発現の増加とともに、胆嚢がんと強く関係している[26]。さらに、COX-2の産物であるPGH2はプロスタグランジンEシンターゼによってPGE2に変換され、がんの進行を促進する。したがって、COX-2の阻害はこれらのタイプのがんの予防と治療に有効である可能性がある[27]。
COX-2の発現はヒトの特発性網膜前膜でもみられる[28]。炎症の急性期にロルノキシカムによってCOXを阻害することで、増殖性硝子体網膜症(PVR)のジスパーゼモデルでは膜形成の頻度が43%、コンカナバリンモデルでは31%低下する。ロルノキシカムは、いずれのPVRモデルにおいてもCOXの発現を正常化しただけでなく、炎症促進因子の注入による網膜や脈絡膜の厚さの変化を抑制した。これらの事実は、PVRの発症におけるCOXとプロスタグランジンの重要性を強調するものである[29]。
PTGS2遺伝子のアップレギュレーションは、ヒトの生殖の複数の段階と関係している。PTGS2遺伝子は、羊膜上皮の絨毛膜板、合胞体性栄養膜、絨毛線維芽細胞、chorionic trophoblast、amniotic trophoblast、胎盤基底板、脱落膜細胞、絨毛外細胞性栄養膜で発現している。絨毛膜羊膜炎/脱落膜炎の過程における羊膜、絨毛脱落膜におけるPTGS2のアップレギュレーションは、子宮内での炎症の3つの限定的な効果の1つである。卵膜におけるPTGS2遺伝子の発現上昇は炎症の存在と関連しており、子宮でのプロスタグランジン遺伝子の発現や、chorionic trophoblast cellや隣接する絨毛膜または絨毛脱落膜へのプロスタグランジン経路タンパク質の免疫局在化を引き起こす。PTGS2(COX-2)は免疫系と関係しており、炎症性白血球で観察される。羊膜でのPTGS2の発現と自然分娩の過程には正の相関が存在し、分娩によって妊娠期間に応じて発現が増加することが発見されているが、胎盤や絨毛脱落膜では早産・正期産に関わらず変化はみられない。また、オキシトシンは子宮筋層細胞でPTGS2の発現を刺激する[30]。
漢族では、PTGS2 5939C変異アレルの保有者は胃がんのリスクが高いことが示されている。また、ピロリ菌Helicobacter pyloriの感染と5939Cアレルの存在との間に関連性が認められている[31]。
相互作用
編集歴史
編集COX-2は1991年にブリガム・ヤング大学のDaniel Simmonsの研究室によって発見された[33]。
出典
編集- ^ a b c GRCh38: Ensembl release 89: ENSG00000073756 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000032487 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ “Human cyclooxygenase-2 cDNA”. Proc. Natl. Acad. Sci. U.S.A. 89 (16): 7384–8. (August 1992). Bibcode: 1992PNAS...89.7384H. doi:10.1073/pnas.89.16.7384. PMC 49714. PMID 1380156.
- ^ “Cyclooxygenase-2: molecular biology, pharmacology, and neurobiology”. Crit Rev Neurobiol 13 (1): 45–82. (1999). doi:10.1615/critrevneurobiol.v13.i1.30. PMID 10223523.
- ^ “Identification and absolute configuration of dihydroxy-arachidonic acids formed by oxygenation of 5S-HETE by native and aspirin-acetylated COX-2”. J. Lipid Res. 51 (3): 575–85. (2010). doi:10.1194/jlr.M001719. PMC 2817587. PMID 19752399.
- ^ “Lipoxins and aspirin-triggered 15-epi-lipoxins are the first lipid mediators of endogenous anti-inflammation and resolution”. Prostaglandins Leukot. Essent. Fatty Acids 73 (3–4): 141–62. (2005). doi:10.1016/j.plefa.2005.05.002. PMID 16005201.
- ^ Wang Q1, He Y, Shen Y, Zhang Q, Chen D, Zuo C, Qin J, Wang H, Wang J, Yu Y. (2014). “Vitamin D inhibits COX-2 expression and inflammatory response by targeting thioesterase superfamily member 4”. J Biol Chem 289 (17): 11681–11694. doi:10.1074/jbc.M113.517581. PMC 4002078. PMID 24619416.
- ^ Kassi E1, Adamopoulos C, Basdra EK, Papavassiliou AG. (2013). “Role of Vitamin D in Atherosclerosis”. Circulation 128 (23): 2517–2531. doi:10.1161/CIRCULATIONAHA.113.002654. PMID 24297817.
- ^ “Prostaglandin endoperoxide H synthases (cyclooxygenases)-1 and -2”. J. Biol. Chem. 271 (52): 33157–60. (December 1996). doi:10.1074/jbc.271.52.33157. PMID 8969167.
- ^ “A mechanistic study of self-inactivation of the peroxidase activity in prostaglandin H synthase-1”. J. Biol. Chem. 274 (14): 9231–7. (April 1999). doi:10.1074/jbc.274.14.9231. PMID 10092596.
- ^ “The kinetic factors that determine the affinity and selectivity for slow binding inhibition of human prostaglandin H synthase 1 and 2 by indomethacin and flurbiprofen”. J. Biol. Chem. 271 (7): 3548–54. (February 1996). doi:10.1074/jbc.271.7.3548. PMID 8631960.
- ^ “Mechanisms for the autoxidation of polyunsaturated lipids”. Accounts of Chemical Research 19 (9): 262–8. (1986). doi:10.1021/ar00129a001.
- ^ “A carbon-centered free radical intermediate in the prostaglandin synthetase oxidation of arachidonic acid. Spin trapping and oxygen uptake studies”. J. Biol. Chem. 255 (11): 5019–22. (June 1980). doi:10.1016/S0021-9258(19)70741-8. PMID 6246094.
- ^ “Identification of novel arachidonic acid metabolites formed by prostaglandin H synthase”. Eur. J. Biochem. 169 (1): 113–23. (November 1987). doi:10.1111/j.1432-1033.1987.tb13587.x. PMID 3119336.
- ^ “Analysis of hydroperoxide-induced tyrosyl radicals and lipoxygenase activity in aspirin-treated human prostaglandin H synthase-2”. Biochemistry 36 (7): 1836–45. (February 1997). doi:10.1021/bi962476u. PMID 9048568.
- ^ “Enzymatic conversions of 10,10-difluoroarachidonic acid with PGH synthase and soybean lipoxygenase”. Journal of the American Chemical Society 109 (12): 3692–3698. (June 1987). doi:10.1021/ja00246a028.
- ^ “Carbocations in the synthesis of prostaglandins by the cyclooxygenase of PGH synthase? A radical departure!”. Protein Sci. 8 (5): 1087–98. (May 1999). doi:10.1110/ps.8.5.1087. PMC 2144324. PMID 10338019.
- ^ “On the mechanism of the biosynthesis of prostaglandins E-1 and F-1-alpha”. J. Biol. Chem. 242 (22): 5336–43. (November 1967). doi:10.1016/S0021-9258(18)99433-0. PMID 6070851.
- ^ a b “Human cyclooxygenase-2 is a sequence homodimer that functions as a conformational heterodimer”. J. Biol. Chem. 286 (21): 19035–46. (May 2011). doi:10.1074/jbc.M111.231969. PMC 3099718. PMID 21467029.
- ^ “The X-ray crystal structure of the membrane protein prostaglandin H2 synthase-1”. Nature 367 (6460): 243–9. (January 1994). Bibcode: 1994Natur.367..243P. doi:10.1038/367243a0. PMID 8121489.
- ^ a b “Cyclooxygenase enzymes: catalysis and inhibition”. Curr. Opin. Struct. Biol. 11 (6): 752–60. (December 2001). doi:10.1016/S0959-440X(01)00277-9. PMID 11751058.
- ^ a b “Cardiomyocyte cyclooxygenase-2 influences cardiac rhythm and function”. Proc. Natl. Acad. Sci. U.S.A. 106 (18): 7548–52. (May 2009). Bibcode: 2009PNAS..106.7548W. doi:10.1073/pnas.0805806106. PMC 2670242. PMID 19376970.
- ^ Ruan, C. H.; So, S. P.; Ruan, K. H. (2011). “Inducible COX-2 dominates over COX-1 in prostacyclin biosynthesis: Mechanisms of COX-2 inhibitor risk to heart disease”. Life Sciences 88 (1–2): 24–30. doi:10.1016/j.lfs.2010.10.017. PMC 3046773. PMID 21035466.
- ^ “Cyclooxygenase-2, p53 and glucose transporter-1 as predictors of malignancy in the development of gallbladder carcinomas”. Bosn J Basic Med Sci 10 (3): 192–6. (August 2010). doi:10.17305/bjbms.2010.2684. PMC 5504494. PMID 20846124.
- ^ “Cyclooxygenase-2 and cancer treatment: understanding the risk should be worth the reward”. Clin. Cancer Res. 16 (5): 1384–90. (March 2010). doi:10.1158/1078-0432.CCR-09-0788. PMC 4307592. PMID 20179228.
- ^ KASE, SATORU; SAITO, WATARU; OHNO, SHIGEAKI; ISHIDA, SUSUMU (2010). “Cyclo-Oxygenase-2 Expression in Human Idiopathic Epiretinal Membrane”. Retina 30 (5): 719–723. doi:10.1097/iae.0b013e3181c59698. PMID 19996819.
- ^ Tikhonovich, Marina V.; Erdiakov, Aleksei K.; Gavrilova, Svetlana A. (2017-06-21). “Nonsteroid anti-inflammatory therapy suppresses the development of proliferative vitreoretinopathy more effectively than a steroid one” (英語). International Ophthalmology 38 (4): 1365–1378. doi:10.1007/s10792-017-0594-3. ISSN 0165-5701. PMID 28639085.
- ^ Phillips, Robert J.; Fortier, Michel A.; López Bernal, Andrés (2014-07-22). “Prostaglandin pathway gene expression in human placenta, amnion and choriodecidua is differentially affected by preterm and term labour and by uterine inflammation”. BMC pregnancy and childbirth 14: 241. doi:10.1186/1471-2393-14-241. ISSN 1471-2393. PMC 4223419. PMID 25048443.
- ^ “A new cyclo-oxygenase-2 gene variant in the Han Chinese population is associated with an increased risk of gastric carcinoma”. Mol Diagn Ther 14 (6): 351–5. (December 2010). doi:10.1007/bf03256392. PMID 21275453.
- ^ “Colocalization and interaction of cyclooxygenase-2 with caveolin-1 in human fibroblasts”. J. Biol. Chem. 276 (37): 34975–82. (September 2001). doi:10.1074/jbc.M105946200. PMID 11432874.
- ^ “Expression of a mitogen-responsive gene encoding prostaglandin synthase is regulated by mRNA splicing”. Proc. Natl. Acad. Sci. U.S.A. 88 (7): 2692–6. (April 1991). Bibcode: 1991PNAS...88.2692X. doi:10.1073/pnas.88.7.2692. PMC 51304. PMID 1849272.
関連文献
編集- “Signaling pathways regulating aromatase and cyclooxygenases in normal and malignant breast cells”. J. Steroid Biochem. Mol. Biol. 80 (2): 203–12. (February 2002). doi:10.1016/S0960-0760(01)00187-X. PMID 11897504.
- “Expression and cellular localization of cyclooxygenases and prostaglandin E synthases in the hemorrhagic brain.”. J Neuroinflammation 8: 22. (2011). doi:10.1186/1742-2094-8-22. PMC 3062590. PMID 21385433.
- “Characterization of cyclooxygenase-2 (COX-2) during tumorigenesis in human epithelial cancers: evidence for potential clinical utility of COX-2 inhibitors in epithelial cancers”. Prostaglandins Leukot. Essent. Fatty Acids 66 (1): 13–8. (January 2002). doi:10.1054/plef.2001.0335. PMID 12051953.
- “Cyclooxygenase-2 and gastric carcinogenesis”. APMIS 111 (10): 915–25. (October 2003). doi:10.1034/j.1600-0463.2003.1111001.x. PMID 14616542.
- “Role of cyclooxygenase-2 in colorectal cancer”. Cancer Metastasis Rev. 23 (1–2): 63–75. (2004). doi:10.1023/A:1025863029529. PMID 15000150.
- “Prevention of head and neck cancer: current status and future prospects”. Curr Probl Cancer 28 (5): 265–86. (2004). doi:10.1016/j.currproblcancer.2004.05.003. PMID 15375804.
- “Chemoprevention in lung cancer”. Curr Probl Cancer 28 (5): 287–306. (2004). doi:10.1016/j.currproblcancer.2004.05.005. PMID 15375805.
- “Cox and mesothelioma: an overview”. Histol. Histopathol. 20 (4): 1267–74. (October 2005). PMID 16136507.
- “Relationship between aromatase and cyclooxygenases in breast cancer: potential for new therapeutic approaches”. Minerva Endocrinol. 31 (1): 13–26. (March 2006). PMID 16498361.
- “Role of cyclooxygenase-2 in the carcinogenesis of gastrointestinal tract cancers: a review and report of personal experience”. World J. Gastroenterol. 12 (9): 1336–45. (March 2006). doi:10.3748/wjg.v12.i9.1336. PMC 4124307. PMID 16552798.
- “The role of the cylooxygenase pathway in nociception and pain”. Semin. Cell Dev. Biol. 17 (5): 544–54. (October 2006). doi:10.1016/j.semcdb.2006.09.001. PMID 17071117.
- “Rofecoxib, Merck, and the FDA”. N. Engl. J. Med. 351 (27): 2875–8; author reply 2875–8. (December 2004). doi:10.1056/NEJM200412303512719. PMID 15625749.
- “Cyclooxygenase‐2, Prostaglandin E2, and Microglial Activation in Prion Diseases”. Cyclooxygenase-2, prostaglandin E2, and microglial activation in prion diseases. International Review of Neurobiology. 82. (2007). 265–75. doi:10.1016/S0074-7742(07)82014-9. ISBN 9780123739896. PMID 17678966