シアヌル酸クロリド
シアヌル酸クロリド(シアヌルさんクロリド、英: Cyanuric chloride)は、化学式(NCCl)3で表される複素環式化合物の一種で、塩化シアヌルとも呼ばれる。1,3,5-トリアジンが塩素化された構造で、塩化シアンの三量体ともみなされる[3]。除草剤の合成原料などとして使用される。
| シアヌル酸クロリド Cyanuric Chloride | |
|---|---|

| |
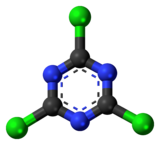
| |
2,4,6-Trichloro-1,3,5-triazine | |
別称 トリクロロトリアジン 塩化シアヌル TCT | |
| 識別情報 | |
| CAS登録番号 | 108-77-0 |
| PubChem | 7954 |
| ChemSpider | 7666 |
| EC番号 | 203-614-9 |
| 国連/北米番号 | 2670 |
| ChEBI | |
| RTECS番号 | XZ1400000 |
| |
| |
| 特性 | |
| 化学式 | C3Cl3N3 |
| モル質量 | 184.41 g mol−1 |
| 外観 | 白色の結晶ないし粉末 |
| 匂い | 刺激臭 |
| 密度 | 1.32 g/cm3 |
| 融点 |
154 °C, 427 K, 309 °F |
| 沸点 |
192 °C, 465 K, 378 °F |
| 水への溶解度 | 400.8mg/L[1] |
| 有機溶媒への溶解度 | アセトン、クロロホルム、トルエンに可溶[2] |
| 構造 | |
| 結晶構造 | 単斜晶 |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 1231 |
| EU分類 | |
| EU Index | 613-009-00-5 |
| NFPA 704 | |
| Rフレーズ | R14, R22, R26, R34, R43 |
| Sフレーズ | (S1/2), S26, S28, S36/37/39, S45, S46, S63 |
| 発火点 | 650℃[2] |
| 半数致死量 LD50 | 485 mg/kg (ラット, 経口) |
| 関連する物質 | |
| 関連するハロゲン化トリアジン | シアヌル酸フルオリド シアヌル酸ブロミド |
| 関連物質 | シアヌル酸 メラミン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
製造
編集シアン化水素から塩化シアンを経て、高温の炭素触媒の存在下で三量化する2段階の合成法で製造される。
2005年には20万トンが製造された[4]。
用途
編集シアヌル酸クロリドの70%が、アトラジンなどのトリアジン系農薬の製造に使用されていると推定される。
他のトリアジン系除草剤のシマジン、アニラジン、シロマジンなども、同様の方法で作られる[5]。また、ビス(トリアジニルアミノ)スチルベンジスルホン酸誘導体をはじめとする、合成洗剤や製紙工程で使用される蛍光染料[4]や架橋剤の前駆体ともなる。多くの反応染料はトリアジン環を有し、塩素の置換反応により製造される[5][6]。
有機合成
編集特殊な用途として、有機合成化学においてアルコールを塩化アルキルに、またカルボン酸をアシル塩化物に変換するための試薬として使用される[7]。
脱水剤や、カルボン酸をアルコールに還元する用途もある。ジメチルホルムアミドとともに加熱すると、ゴールド試薬( Me2NCH=NCH=NMe2+Cl− )を生じる。これは、アミノアルキル化剤の原料や複素環式化合物の前駆体となる[8][9]。
塩素は容易にアミンに置換され、メラミンの誘導体を与える。デンドリマーなどの合成に使われる[10][11]。
また、アデノシン受容体の実験的な合成において、リガンドとして使用される。[12]
脚注
編集- ^ 製品安全データシート(厚生労働省 職場のあんぜんサイト)
- ^ a b シアヌル酸クロリド(東京化成工業)
- ^ Cyanuric chloride at Chemicalland21.com
- ^ a b Klaus Huthmacher, Dieter Most "Cyanuric Acid and Cyanuric Chloride" in Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a08_191.
- ^ a b Ashford's Dictionary of Industrial Chemicals, 3rd edition, 2011, pages 2495-8
- ^ Horst Tappe, Walter Helmling, Peter Mischke, Karl Rebsamen, Uwe Reiher, Werner Russ, Ludwig Schläfer and Petra Vermehren "Reactive Dyes"in Ullmann's Encyclopedia of Industrial Chemistry 2000, Wiley-VCH, Weinheim. doi:10.1002/14356007.a22_651
- ^ K. Venkataraman, and D. R. Wagle (1979). “Cyanuric chloride : a useful reagent for converting carboxylic acids into chlorides, esters, amides and peptides”. Tet. Lett. 20 (32): 3037–3040. doi:10.1016/S0040-4039(00)71006-9.
- ^ Probst, D. A.; Hanson, P. R.; Barda, D. A. "Cyanuric Chloride" in Encyclopedia of Reagents for Organic Synthesis, 2004, John Wiley & Sons. doi:10.1002/047084289X.rn00320
- ^ John T. Gupton; Steven A. Andrews (1990). "β-Dimethylaminomethylenation: N,N-Dimethyl-N'-p-tolylformamidine". Organic Syntheses (英語).; Collective Volume, vol. 7, p. 197
- ^ Abdellatif Chouai and Eric E. Simanek (2008). “Kilogram-Scale Synthesis of a Second-Generation Dendrimer Based on 1,3,5-Triazine Using Green and Industrially Compatible Methods with a Single Chromatographic Step”. J. Org. Chem. 73 (6): 2357–2366. doi:10.1021/jo702462t. PMID 18307354.
- ^ Reagent: DIPEA, amine protective group: BOC
- ^ WO application 03101980, "1,3,5-TRIAZINE DERIVATIVES AS LIGANDS FOR HUMAN ADENOSINE-A3 RECEPTORS", published 2003-12-11 (Reagent number two: norephedrine, base DIPEA)
- ^ De Luca, L.; Giacomelli, G.; Procheddu, A (2001). “A Mild and Efficient Alternative to the Classical Swern Oxidation”. J. Org. Chem: 7907. doi:10.1021/jo015935s.
- ^ 2,4,6-トリクロロ-1,3,5-トリアジン (PDF) (財団法人化学物質評価研究機構)
